Servizi globali
Identificazione unica del dispositivo (UDI)
Il 24 settembre 2013, la Food and Drug Administration (FDA) degli Stati Uniti ha approvato una norma definitiva che impone alla maggior parte dei dispositivi medici distribuiti negli USA di essere dotati di Identificatori unici (UDI). Il sistema UDI agevola l'identificazione, la tracciabilità e il monitoraggio dei dispositivi medici dalla distribuzione all'uso. In base alla norma, le informazioni sui prodotti riguardanti i dispositivi devono essere inviate al Global Unique Device Identification Database (GUDID) della FDA.
In base alla norma, inoltre, tutte le etichette dei dispositivi medici devono usare un nuovo formato data uniformato.
Masimo ha aggiornato le sue etichette per adeguarsi alla normativa UDI e agli Standard GS1.
Per fare ulteriori domande, contatta l'Assistenza clienti.
USA: customerorders@masimo.com
Altri Paesi: emeasales@masimo.com
1. Cosa è l'UDI?
Un Identificatore unico del dispositivo (UDI) è costituito da una serie di caratteri numerici o alfanumerici, basati su un criterio di codifica globale che identifica adeguatamente un dispositivo dalla distribuzione all'uso. È composto da:
- un identificatore del dispositivo, cioè il GTIN (Global Trade Item Number, numero elemento commerciale globale), una parte invariabile e obbligatoria dell'UDI che identifica la specifica versione o il modello del dispositivo e il relativo etichettatore; e
- un identificatore di produzione, cioè una parte variabile e subordinata dell'UDI che identifica una o più delle seguenti voci, quando compresa nell'etichetta del dispositivo:
- il lotto di produzione del dispositivo;
- il numero di serie di uno specifico dispositivo;
- la data di scadenza di uno specifico dispositivo; e/o
- la data di produzione di uno specifico dispositivo.
L'agenzia accreditata di Masimo per l'assegnazione di codici a barre e relative strutture è GS1 .
I prodotti NON classificati come dispositivi medici non devono necessariamente contenere un codice a barre.
2. Chi deve attenersi alle normative UDI?
Tutte le aziende produttrici di dispositivi medici devono attenersi alle normative UDI.
3. Qual è la sequenza temporale di applicazione per uniformarsi alle normative UDI?
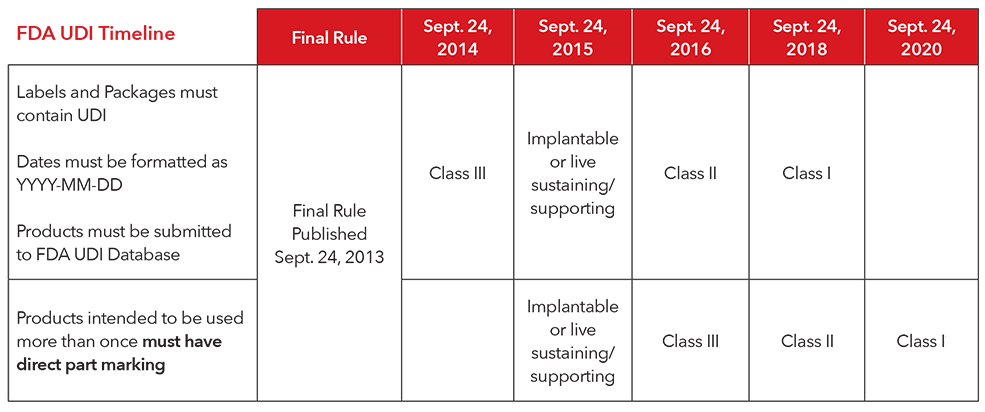
4. Come Masimo si adegua alle normative UDI?
Masimo distribuisce prodotti di Classe II e qualche prodotto di Classe I. Masimo ha aggiornato le sue etichette per adeguarsi alla normativa UDI e agli Standard GS1.
I prodotti NON classificati come dispositivi medici non devono necessariamente contenere un codice a barre.
5. Come saranno la mia etichetta UDI e la marcatura diretta delle parti?
Esempi:
- Etichette scatole sensori con versione precedente ed etichette UDI aggiornate
- Sensore con marcatura diretta delle parti
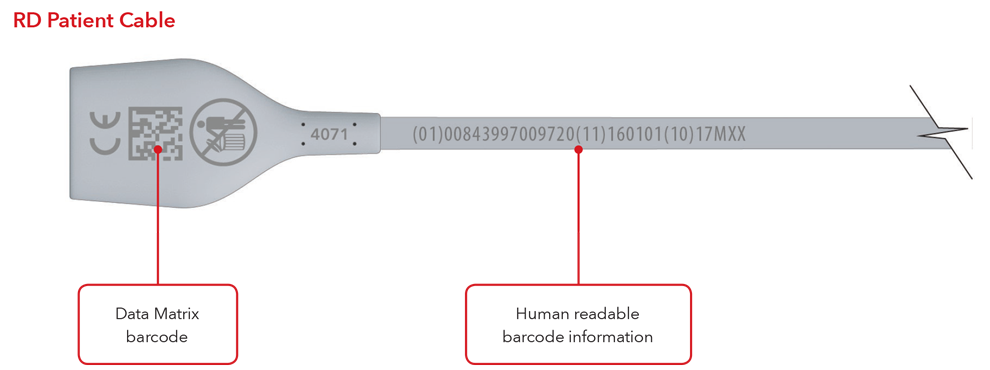
- Cavo con marcatura diretta delle parti
Nota: in base al tipo di prodotto, l'etichetta contiene una di due date. Per i prodotti con data "Usare entro", appare come AAAA-MM-GG sotto il simbolo della scadenza ed è anche codificata come AAMMGG, preceduta dall'identificatore di produzione (17) nei codici a barre GS1 2 2D. Per i prodotti senza data "Usare entro", la data di produzione appare come AAAA-MM-GG accanto al simbolo della data di produzione ed è anche codificata come AAMMGG, preceduta dall'identificatore di produzione (11) nei codici a barre GS1 e 2D.
Esempi di etichette scatole sensori
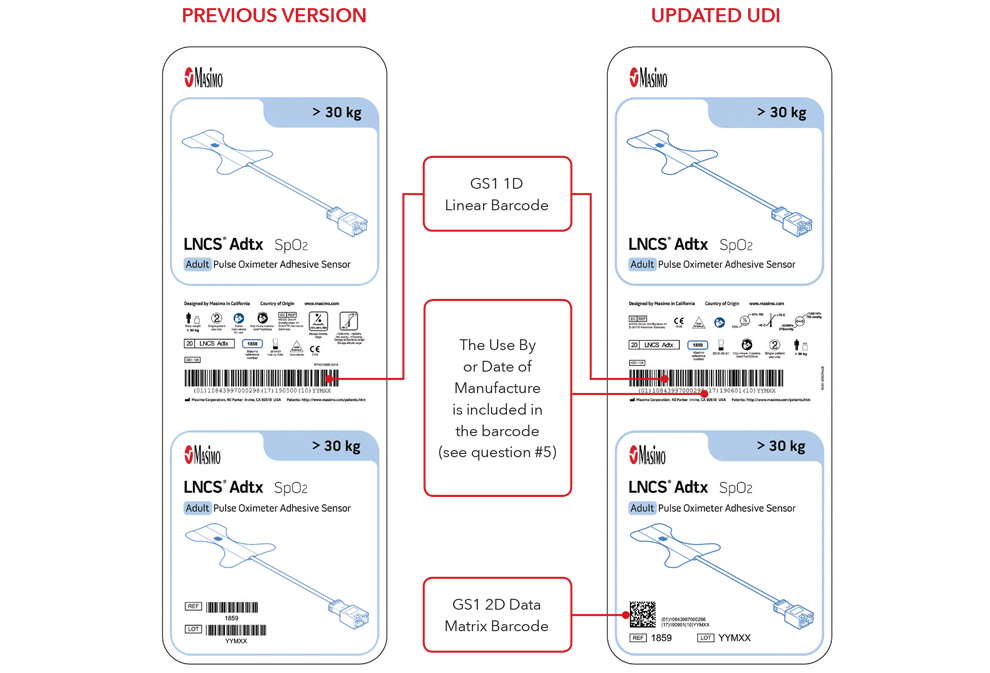
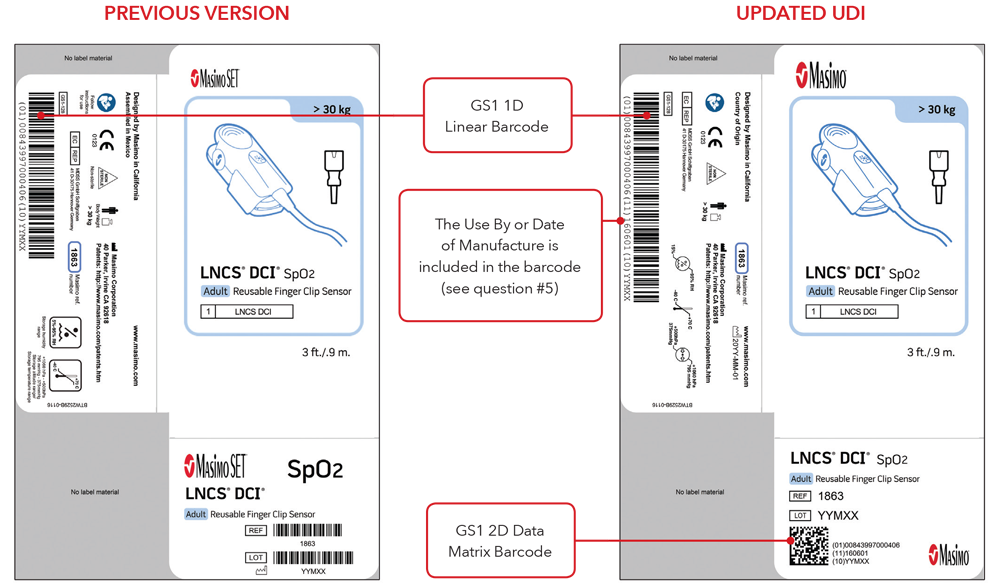
Esempi di sensori e cavi con marcatura diretta delle parti
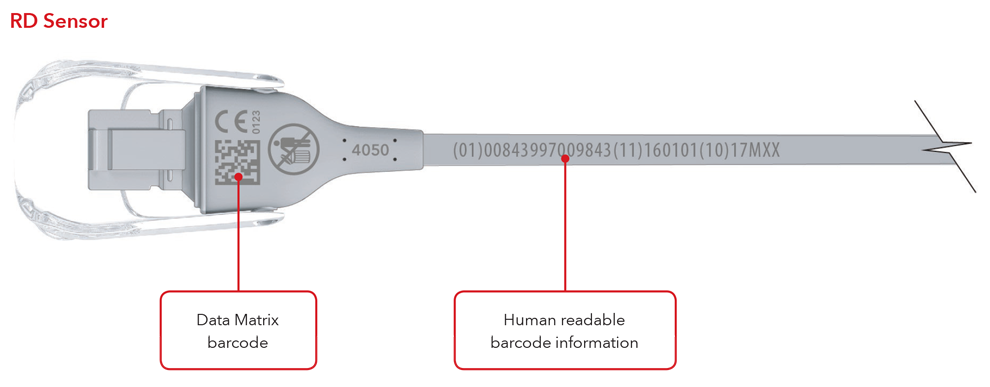
6. Cosa è il Global Trade Item Number (GTIN)?
Il GTIN è un numero di identificazione GS1 globalmente unico, usato per identificare un "elemento commerciale". I GTIN sono assegnati dal titolare del marchio (etichettatore) del prodotto e sono usati per identificare i prodotti destinati all'utente finale (ad esempio un ospedale) attraverso la catena di approvvigionamento globale. Se attualmente non usi il sistema GS1 con i GTIN per gestire i tuoi prodotti, devi ottenere i GTIN per i prodotti da vendere.
Per ulteriori informazioni sui GTIN, contatta GS1 su https://www.gs1us.org/what-we-do/standards.
7. Come posso ottenere i GTIN per i prodotti?
Invia una e-mail all'Assistenza clienti di Masimo:
USA: customerorders@masimo.com
Altri Paesi: emeasales@masimo.com
Scrivi anche il tuo ID cliente e il o i numeri di parte dei prodotti nell'e-mail.
8. Attualmente inserisco o effettuo la scansione dei codici a barre LOTTO e/o RIF di Masimo sull'etichetta. Ci saranno disagi?
Sì. I codici a barre LOTTO o RIF sull'etichetta saranno sostituiti con testi e non potranno più essere scansionati. Le informazioni sul LOTTO, per le quali si potrà fare la scansione del codice a barre GS1, saranno disponibili anche accanto al simbolo del LOTTO sull'etichetta. Le informazioni sul RIF possono essere individuate nel corrispondente GTIN. Per ulteriori informazioni sui GTIN, vedere la domanda n. 6 sopra.
9. I numeri di prodotto di Masimo cambieranno a causa dell'applicazione delle normative UDI?
No, rimarranno uguali.
10. Cosa è il nuovo formato data uniformato e quando entrerà in vigore?
La norma UDI ha adottato il formato data uniformato AAAA-MM-GG sulle etichette dei dispositivi. Le date sulle etichette passeranno al nuovo formato non più tardi di quando l'etichetta sul dispositivo dovrà riportare l'UDI. Per ulteriori informazioni sulla sequenza temporale di applicazione, vedere la domanda n. 3 sopra.
11. Masimo fornirà informazioni sui prodotti online?
Il GUDID è un database di ricerca pubblico che contiene la parte di identificazione del dispositivo (DI) dell'UDI per ogni dispositivo medico nonché altre informazioni necessarie sul prodotto. Tutte le aziende produttrici di dispositivi medici devono inviare le informazioni DI al GUDID. Masimo ha iniziato a riempire il GUDID e verificherà che tutti i prodotti siano aggiunti conformemente alla sequenza temporale di applicazione dell'UDI o prima.
12. Cosa ne sarà delle giacenze esistenti? I produttori dovranno eseguire una nuova marcatura?
No. Per le giacenze esistenti ci sono due possibilità:
- I dispositivi distribuiti in commercio prima della data di conformità applicabile non devono uniformarsi alla norma definitiva.
- Anche i dispositivi prodotti ed etichettati prima della data di conformità applicabile non devono uniformarsi alla norma definitiva. In questo caso però l'eccezione scade 3 anni dopo la data di conformità applicabile.
13. Tutti i dispositivi devono essere direttamente marchiati con il relativo UDI?
No. La norma impone solo la marcatura diretta ai dispositivi medici riutilizzabili che devono essere ritrattati (pulizia di alto livello/sterilizzazione) prima dell'uso.
Per ulteriori informazioni sulla sequenza temporale di applicazione della marcatura diretta, vedere la domanda n. 3 sopra.
Per ulteriori informazioni sul sistema UDI, vedere Identificazione unica del dispositivo (UDI) sul sito web della FDA:
http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/UniqueDeviceIdentification/
Per fare ulteriori domande su come Masimo si adegua alle normative UDI, contatta l'Assistenza clienti di Masimo:
USA: customerorders@masimo.com
Altri Paesi: emeasales@masimo.com
PLCO-008044/ PLMM-12788A-0326 EN- PLMM-10045D